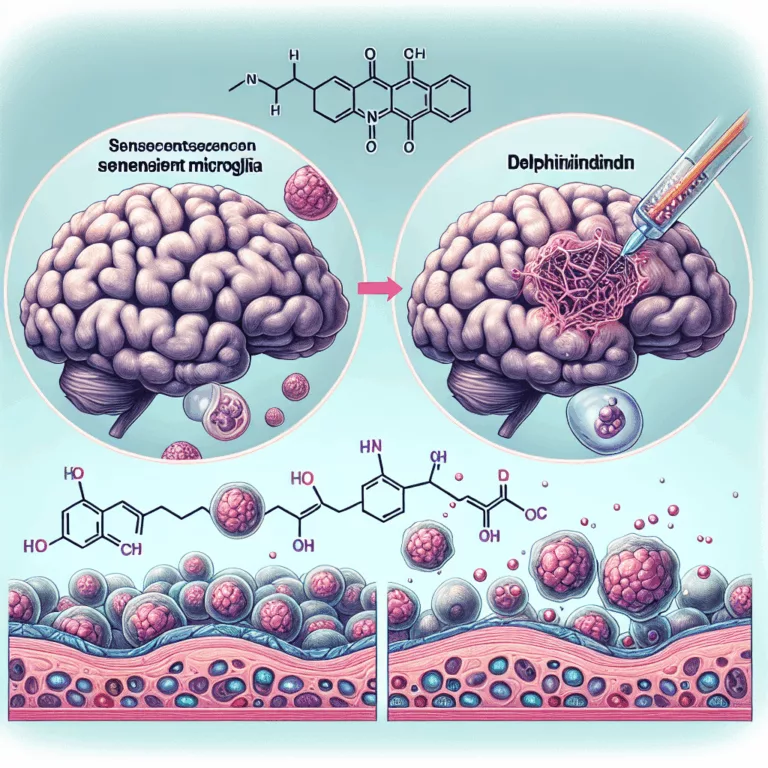
Rôle des Microglies Sénescentes dans la Maladie d’Alzheimer et l’Efficacité de la Delphinidine
Les microglies sont des cellules immunitaires innées du cerveau, comparables aux macrophages dans le reste du corps. Des recherches récentes montrent que le comportement inflammatoire maladaptatif des microglies dans le cerveau vieillissant joue un rôle crucial dans l’apparition et la progression de maladies neurodégénératives comme la maladie d’Alzheimer. Certaines microglies deviennent inflammatoires en réponse à…