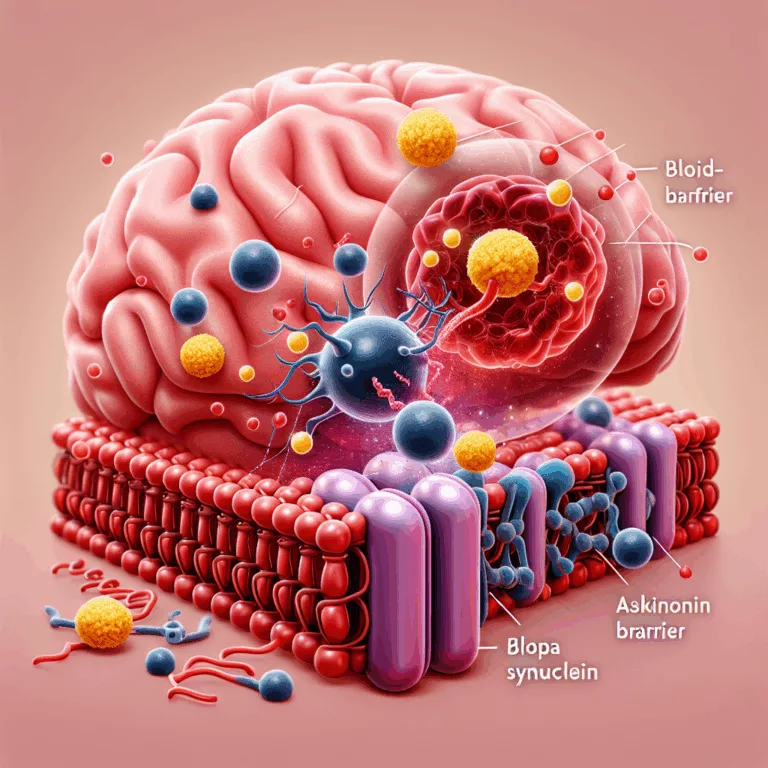
Impact de l’α-synucléine sur la barrière hémato-encéphalique et son implication dans la maladie de Parkinson
Les chercheurs ont découvert comment la protéine α-synucléine (α-syn), impliquée dans la maladie de Parkinson et la démence à corps de Lewy, entraîne une inflammation et une perturbation des axones dans le cerveau. Le cerveau est protégé par une barrière hémato-encéphalique (BHE) qui empêche de nombreuses substances dans le sang d’endommager les neurones. Les dommages…