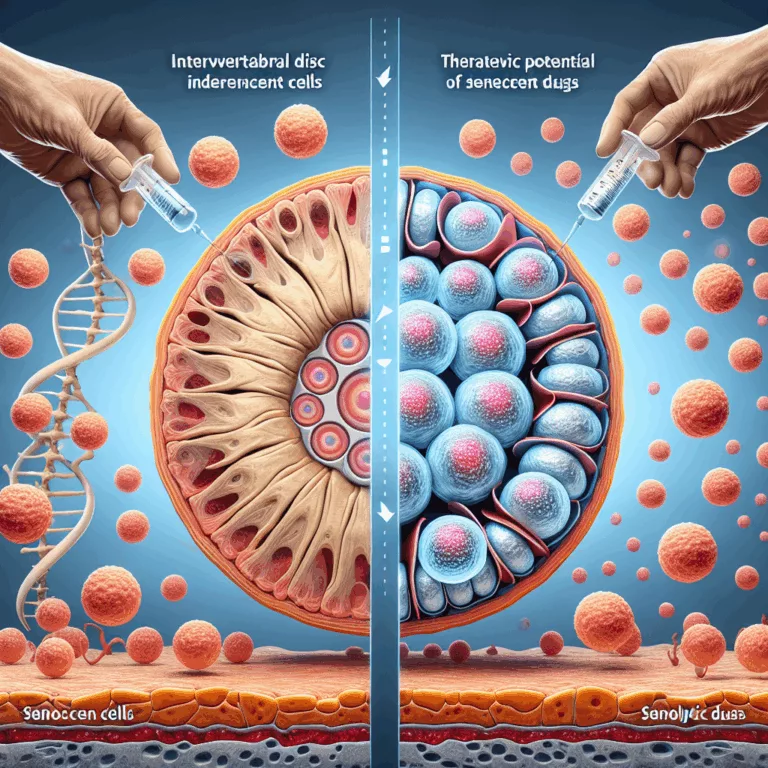
Impact des cellules sénescentes sur la dégénérescence des disques intervertébraux et potentiel thérapeutique des médicaments sénolytiques
Un nombre croissant de travaux suggère que l’accumulation de cellules sénescentes contribue à la dégénérescence fonctionnelle et structurelle des disques intervertébraux (DIV) dans la colonne vertébrale. Ce phénomène est particulièrement préoccupant, car il est à l’origine de douleurs et de pertes fonctionnelles. La capacité de restaurer ces fonctions perdues est très limitée, mais l’élimination des…