L’impact du microbiome intestinal sur le vieillissement et la santé : Une exploration essentielle
Découvrez comment le microbiome intestinal influence la santé et le vieillissement, et les innovations prometteuses dans ce domaine crucial.
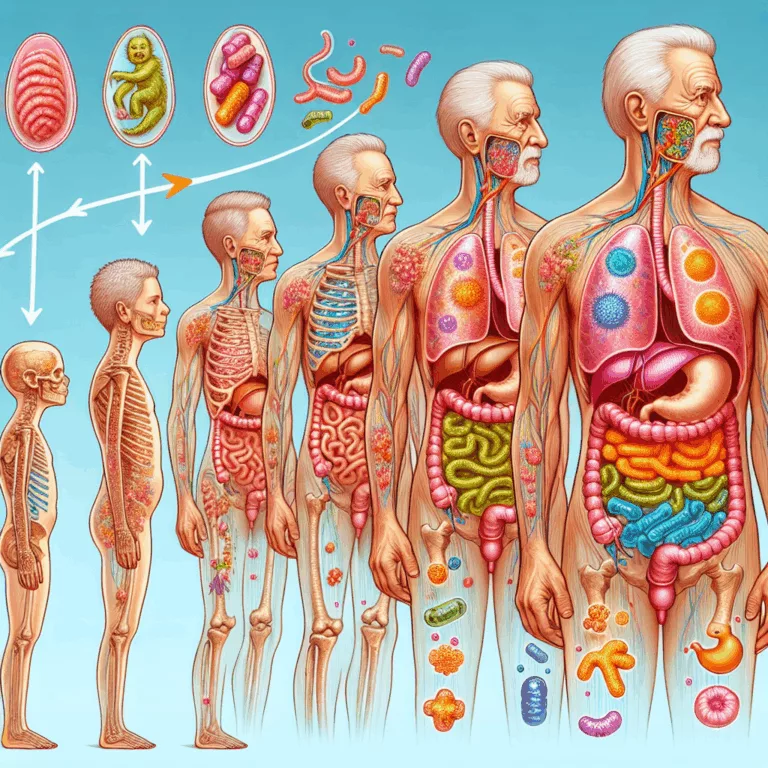
Découvrez comment le microbiome intestinal influence la santé et le vieillissement, et les innovations prometteuses dans ce domaine crucial.
Découvrez comment la sénescence cellulaire influence la santé liée à l’âge et son rôle dans l’inflammation chronique.

Découvrez comment les thérapies systémiques pourraient transformer le traitement des maladies chroniques et le vieillissement en ciblant les réseaux biologiques.

Découvrez comment le canagliflozine influence le vieillissement cérébral et le potentiel de lutte contre la maladie d’Alzheimer chez les souris.

Découvrez comment le fitness cardiorespiratoire influence la santé, la longévité et réduit les risques de multimorbidité.

Découvrez comment les dernières innovations médicales ciblent les mécanismes du vieillissement pour améliorer la longévité et la santé des personnes âgées.

Découvrez le Botticelli, la plateforme laser innovante qui transforme le rajeunissement cutané avec une approche multi-longueurs d’onde.

Découvrez comment l’investissement dans la longévité saine peut transformer nos sociétés et stimuler la prospérité économique mondiale.

Découvrez comment Telomir-1 pourrait révolutionner le traitement des maladies dégénératives grâce à ses effets sur les cellules humaines.

Découvrez comment l’astroimmunologie révèle le lien entre le vol spatial et le déclin immunitaire, avec des implications pour la longévité sur Terre.