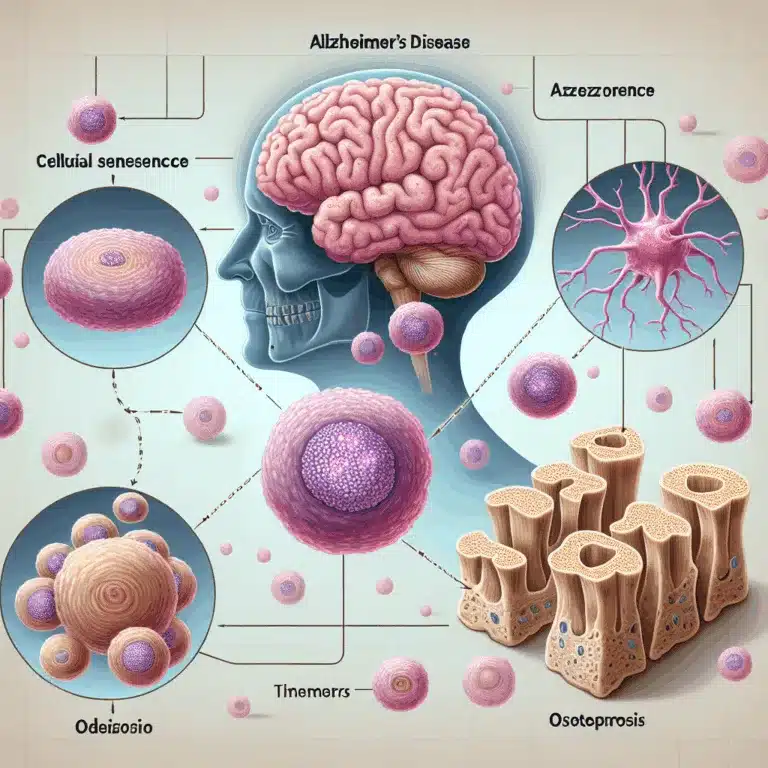
Découverte de liens entre la maladie d’Alzheimer, la sénescence cellulaire et l’ostéoporose
Des chercheurs publiant dans Nature Aging ont découvert un lien entre les agrégats protéiques liés à la maladie d’Alzheimer, les cellules sénescentes et l’ostéoporose. La perte de protéostasie, qui fait référence à la défaillance des mécanismes de construction des protéines dans les cellules, est liée à l’accumulation de protéines mal repliées et est considérée comme…