L-Nutra : Une Révolution dans la Nutrition pour la Longévité et la Gestion du Poids
Découvrez comment L-Nutra transforme la nutrition en solutions durables pour la gestion du poids et du diabète grâce à des innovations cliniques.

Découvrez comment L-Nutra transforme la nutrition en solutions durables pour la gestion du poids et du diabète grâce à des innovations cliniques.

Découvrez comment l’activité physique influence les bénéfices de la restriction calorique sur la santé et la longévité des individus.
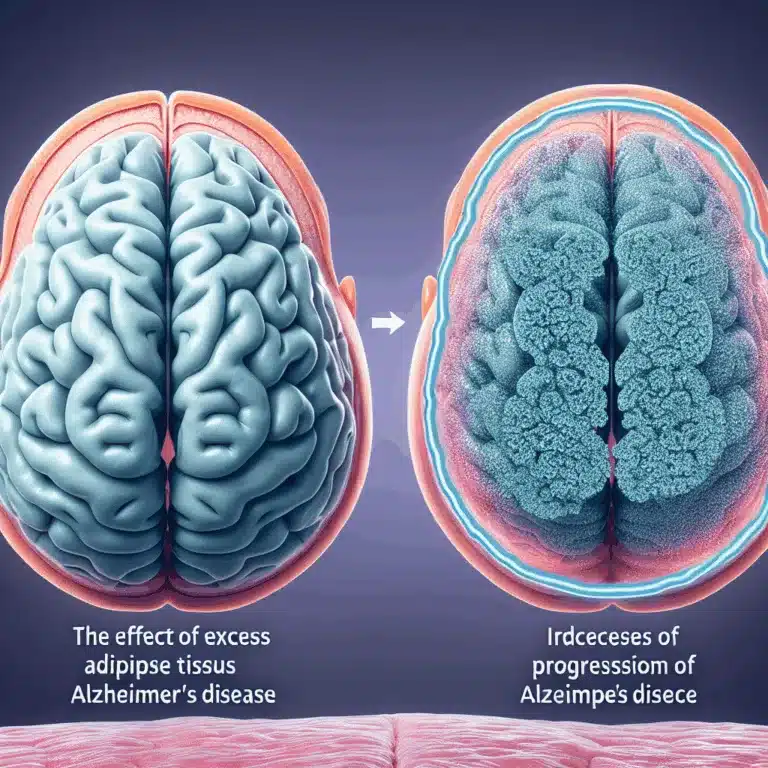
Découvrez comment l’excès de tissu adipeux influence la progression de la maladie d’Alzheimer et son lien avec l’inflammation et la neurodégénérescence.

Rona Therapeutics innove avec RN3161, un siRNA prometteur contre l’obésité ciblant le gène INHBE. Découvrez son potentiel révolutionnaire pour la santé métabolique.

Découvrez comment les GLP-1s pourraient révolutionner la longévité et redéfinir notre approche du vieillissement dans l’industrie pharmaceutique.
Découvrez comment les sous-types de macrophages influencent le vieillissement et l’obésité, révélant des liens surprenants entre inflammation et régénération.

Découvrez comment l’accord entre Phoenix et MD Anderson révolutionne les thérapies cellulaires et ouvre de nouvelles perspectives en médecine de longévité.
Novo Nordisk, un géant pharmaceutique danois, a récemment présenté des données réelles suggérant que son médicament contre l’obésité, Wegovy, réduit considérablement le risque d’événements cardiovasculaires graves chez les personnes souffrant d’obésité et de maladies cardiaques établies. Les résultats de l’étude STEER, dévoilés lors du Congrès de la Société Européenne de Cardiologie à Madrid, ont montré…
Une étude menée par le Buck Institute révèle que les moments clés de la reproduction chez les femmes, tels que l’âge de la première menstruation et de la première grossesse, influencent les trajectoires de santé à long terme. En utilisant la randomisation mendélienne et des données provenant de près de 200 000 femmes dans le…

BioAge Labs, Inc. est une entreprise de biotechnologie en phase clinique qui développe des candidats thérapeutiques pour des maladies métaboliques en ciblant la biologie du vieillissement humain. Récemment, la société a annoncé que le premier participant avait été traité dans un essai clinique de phase 1 évaluant BGE-102, un inhibiteur de NLRP3 oral, novateur et…