La sénescence cellulaire et son impact sur la santé cardiovasculaire : enjeux et perspectives
Découvrez comment la sénescence cellulaire influence les maladies cardiovasculaires et explorez des approches thérapeutiques innovantes.
Découvrez comment la sénescence cellulaire influence les maladies cardiovasculaires et explorez des approches thérapeutiques innovantes.

Découvrez comment l’industrie pharmaceutique peut révolutionner le traitement du vieillissement, en surmontant ses défis actuels et en redéfinissant l’avenir des thérapies.
Découvrez comment le fisetin, agent sénolytique prometteur, pourrait transformer la lutte contre la sénescence cellulaire et améliorer la fonction endothéliale.

Introduction Les maladies cardiovasculaires (MCV) et la démence représentent deux des défis de santé mondiaux les plus pressants, en particulier dans les pays à revenu faible et intermédiaire. Des études épidémiologiques démontrent une forte corrélation entre l’incidence des MCV et celle de la démence. Cette relation suggère qu’il existe un mécanisme causal possible, comme la…
Les chercheurs analysent les variantes génétiques humaines dans le gène IL-6 pour montrer qu’une activité réduite de l’IL-6 est corrélée à un risque plus faible de maladies cardiovasculaires. L’IL-6 circulant est généralement considéré comme un signal pro-inflammatoire, et il représente une cible pour le développement de thérapies. L’inflammation chronique à un âge avancé contribue de…
Novo Nordisk, un géant pharmaceutique danois, a récemment présenté des données réelles suggérant que son médicament contre l’obésité, Wegovy, réduit considérablement le risque d’événements cardiovasculaires graves chez les personnes souffrant d’obésité et de maladies cardiaques établies. Les résultats de l’étude STEER, dévoilés lors du Congrès de la Société Européenne de Cardiologie à Madrid, ont montré…
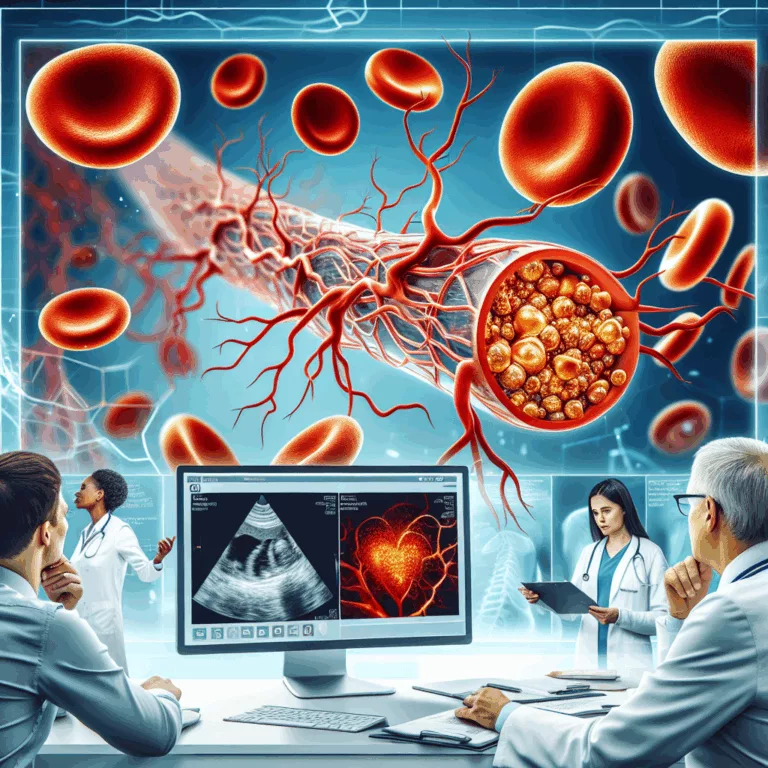
La recherche sur l’athérosclérose est cruciale car cette maladie cardiovasculaire est l’une des principales causes de mortalité dans le monde, résultant de l’accumulation de plaques dans les artères. Un article récent de Cyclarity Therapeutics présente le médicament UDP-003, qui vise à traiter la cause profonde de l’athérosclérose plutôt que de se concentrer uniquement sur ses…
Ces dernières années, la recherche a mis en évidence l’influence de la composition du microbiome intestinal sur la santé à long terme ainsi que sur le vieillissement et les affections liées à l’âge. Des études ont établi des corrélations entre des espèces microbiennes spécifiques et des conditions de santé, montrant que l’ajustement de l’équilibre des…

Le vieillissement est le résultat d’une accumulation de dommages, avec les maladies liées à l’âge étant les dysfonctionnements les plus visibles de cette dégradation. Au fil du temps, l’une de ces dysfonctions devient suffisamment grave pour entraîner la mort. Pour vivre plus longtemps, il est essentiel de réduire la charge de dommages subis par l’organisme,…
Dans la revue Cell Reports Medicine, des chercheurs examinent en détail la relation entre les maladies cardiovasculaires et une inflammation liée à l’âge, connue sous le nom d’inflammaging. Ce phénomène est caractérisé par une inflammation systémique difficile à détecter qui s’intensifie avec l’âge. L’inflammaging affecte non seulement le système immunitaire, mais également le cœur. Les…