Rôle de l’IL-33 dans la progression de l’arthrose et stratégie thérapeutique par nanoparticules
Découvrez comment l’IL-33 influence l’arthrose et explorez une stratégie innovante avec des nanoparticules pour ralentir sa progression.
Découvrez comment l’IL-33 influence l’arthrose et explorez une stratégie innovante avec des nanoparticules pour ralentir sa progression.

Découvrez comment les agrégations protéiques influencent les maladies neurodégénératives et la recherche d’une autophagie améliorée pour préserver notre cerveau.

Introduction Anavex Life Sciences a récemment présenté les résultats de son essai clinique de Phase IIb/III sur l’Alzheimer, où un traitement quotidien de 30 mg de blarcamesine a montré des résultats cognitifs prometteurs dans une population ciblée par une approche de médecine de précision, désignée ABCLEAR3. Selon la société, ces résultats se rapprochent du vieillissement…
Les lysosomes sont des organites essentiels au sein des cellules, servant de systèmes de recyclage grâce à des enzymes capables de décomposer les protéines et les structures cellulaires en matières premières réutilisables. Le processus d’autophagie (optimiser l’autophagie par le jeûne) est responsable de l’identification des protéines et des structures à recycler, qui sont ensuite livrées…
AutoPhagyGO, une entreprise japonaise, est l’une des équipes semi-finalistes du concours XPRIZE Healthspan, qui vise à prouver que le vieillissement n’est pas immuable mais modifiable. En mettant l’accent sur l’autophagie (optimiser l’autophagie par le jeûne), un processus cellulaire reconnu par le prix Nobel, ainsi que sur des interventions de mode de vie ancrées dans la…
La restriction calorique est une pratique consistant à réduire l’apport calorique tout en maintenant des niveaux adéquats de micronutriments. Une réduction de 10 % par rapport aux niveaux recommandés est considérée comme modérée, mais des réductions allant jusqu’à 40 % sont possibles avec suffisamment de diligence. Cette restriction entraîne des changements métaboliques majeurs qui améliorent…

La recherche sur la biologie cellulaire implique souvent la désactivation de gènes afin d’observer leur rôle dans divers processus. Cette méthode peut s’avérer complexe, car les cellules disposent de plusieurs mécanismes pour atteindre un même but, ce qui rend difficile l’analyse des conséquences de la suppression d’un gène. Néanmoins, lorsque l’on identifie un gène essentiel,…

Les cellules réagissent à une large gamme de stress de manière assez similaire. Que ce soit le froid, la chaleur, le manque de nutriments, le manque d’oxygène, la présence de toxines ou l’irradiation, ces facteurs peuvent avoir différents capteurs et réponses initiales, mais ces réponses convergent vers une augmentation des processus de maintenance et de…
Le vieillissement est un processus complexe caractérisé par l’accumulation de dommages cellulaires et tissulaires, ainsi que par les dysfonctionnements qui en résultent. Bien que les dommages liés au vieillissement se produisent indépendamment de l’environnement, les expositions environnementales peuvent également contribuer à ces dommages, donnant l’impression d’un vieillissement accéléré. L’exposition aux rayons ultraviolets (UV), qui provoque…
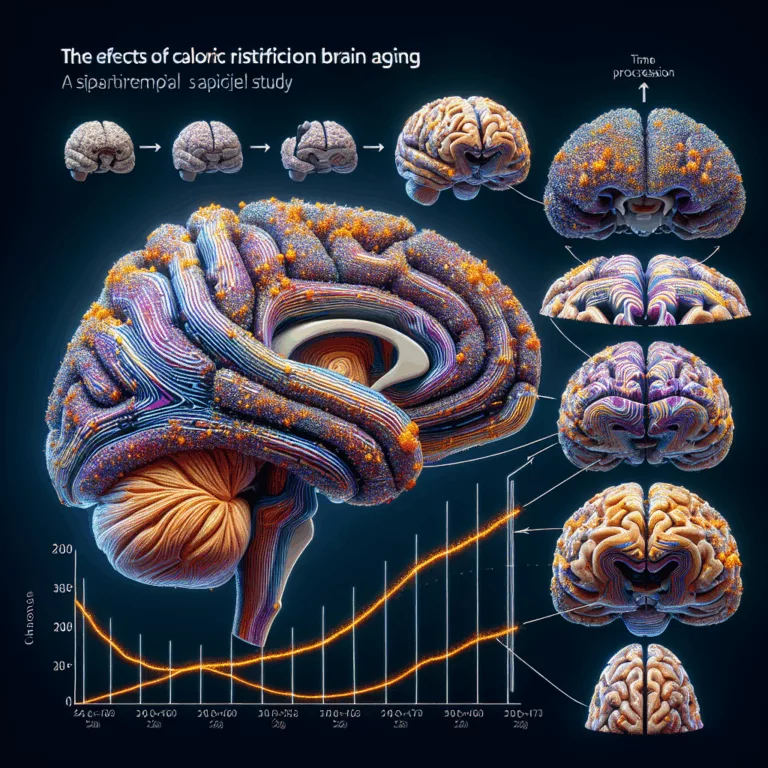
La restriction calorique, qui consiste à réduire sa consommation de calories de 40 % tout en maintenant un apport adéquat en micronutriments, est bien établie comme un moyen de ralentir le vieillissement chez de nombreuses espèces, notamment dans le cas des espèces à courte durée de vie. Des études humaines ont démontré que même une…