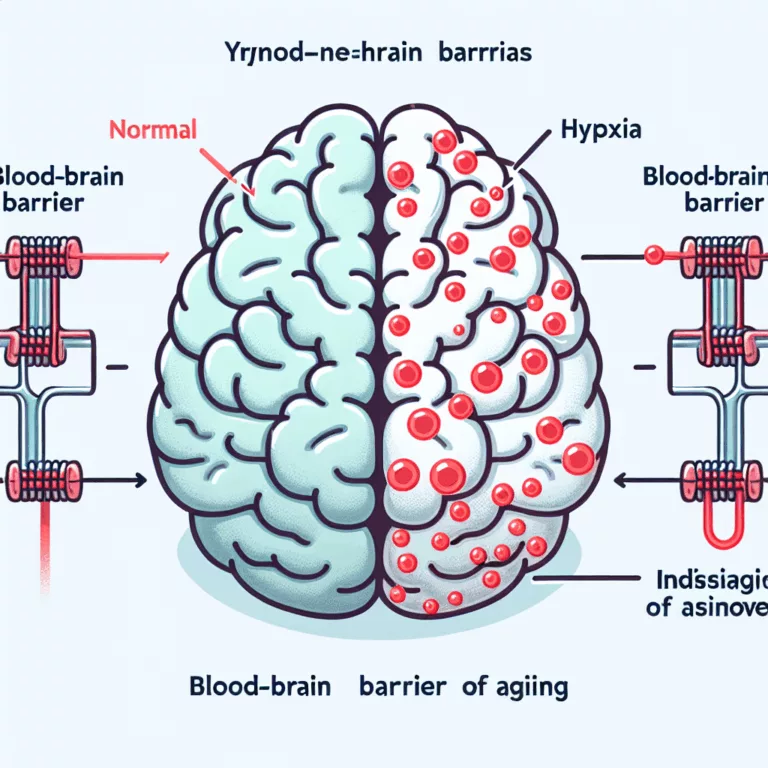
Impact de l’Hypoxie sur la Barrière Hémato-Encéphalique et le Vieillissement
La barrière hémato-encéphalique est composée de cellules spécialisées qui tapissent les vaisseaux sanguins du cerveau. Ces cellules permettent le passage de certaines molécules entre le cerveau et le reste du corps, maintenant ainsi une biochimie distincte et des populations cellulaires spécifiques au système nerveux central. Lorsque la barrière hémato-encéphalique fuit, cela entraîne une inflammation et…